課程內容
《來自石油和煤的兩種基本化工原料》
已知乙烯的密度在標準狀況下是1.25g/L,含碳85.7%,含氫14.3%。利用這些數據怎樣確定乙烯的分子式?
一、乙烯的結構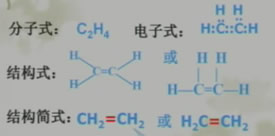
二、比較C2H6和C2H4
C2H6:碳碳鍵型C-C;分子內各原子的相對位置:2個碳原子和6個氫原子不在同一平面
C2H4:碳碳鍵型C=C;分子內各原子的相對位置:2個碳原子和4個氫原子在同一平面
結構小結:
1、C=C雙鍵中有一個鍵不穩定,容易斷裂,有一個鍵比較穩定。
2、鏈烴分子里含有碳碳雙鍵的不飽和烴稱為烯烴。
3、乙烯是最簡單的烯烴。
三、乙烯的物理性質
乙烯是無色無味的氣體;在水中難溶于水,密度較空氣略小。
乙烯的化學性質
乙烯分子中碳碳雙鍵(C=C)里的一個鍵容易斷裂。所以乙烯的化學性質比較活潑。
1、氧化反應
(1)將乙烯氣體點燃
現象:明亮火焰并伴有黑煙(產生黑煙是因為含碳量高,燃燒不充分;火焰明亮是碳微粒受灼熱而發光)
CH2=CH2+3O2→(點燃)2CO2+2H2O
(2)與酸性KMnO4的作用:將乙烯通入酸性KMnO4溶液中:
現象:紫色褪去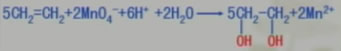
2、加成反應
(1)將乙烯氣體通入溴水溶液中。現象:紅棕色褪去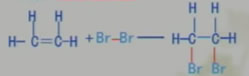
定義:有機物分子中雙鍵(或三鍵)兩端的碳原子與其他原子或原子團直接結合生成新的化合物的反應,叫做加成反應。
(2)與H2、HBr、H2O、HCN反應
3、聚合反應
乙烯聚合過程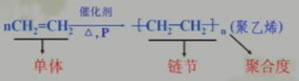
相對分子質量小的化合物分子互相結合成相對分子質量大的高分子的反應叫聚合反應。聚合反應同時也是加成反應的叫加成聚合反應,簡稱加聚反應。
此內容正在抓緊時間編輯中,請耐心等待
劉老師
男,中教高級職稱
工作勤奮,責任心強,多次被評為市優秀教師。